Forskere ved Johns Hopkins Kimmel Cancer Center utvikler en ny blodprøveteknologi kjent som GEMINI (Genome-wide Mutational Incidence for Non-Invasive detection of cancer).
Ved å kombinere genomomfattende sekvensering av enkelt-DNA-molekyler som er blitt forkastet av svulster, med maskinlæring (ML), kan testen gjøre det mulig å oppdage lungekreft og andre kreftformer på et tidligere stadium.
GEMINI-testen analyserer cellefritt DNA (cfDNA) fra svulster, og bruker ML til å oppdage forskjeller i mutasjonsfrekvenser for kreft og ikke-kreft på tvers av genomet. Høyere poengsummer generert av modellen antyder en høyere sannsynlighet for å ha kreft.
I laboratorietester ble GEMINI brukt på datatomografibilder og oppdaget over 90% lungekrefttilfeller, selv i tidlige stadier. Den studie funnene ble publisert i Nature Genetics.
Forskerne fokuserte hovedsakelig på påvisning av lungekreft i høyrisikopopulasjoner.
Det ble imidlertid også observert endrede mutasjonsprofiler i cfDNA fra pasienter med leverkreft, føflekkreft og lymfom, så denne metoden kan brukes på tvers av ulike krefttyper.
Slik skapte forskerne GEMINI
For å utvikle GEMINI studerte teamet genomsekvenser fra 2511 personer med 25 ulike kreftformer.
Ulike svulsttyper hadde forskjellige mutasjonsprofiler. Forskerne fant at genomiske regioner med høy mutasjonsfrekvens var like mellom tumorvev og cfDNA fra blod hos pasienter med lungekreft, melanom eller B-celle non-Hodgkin-lymfom.
GEMINI-testen ble deretter brukt på cfDNA fra 365 personer med høy risiko for lungekreft, og ga høyere score hos personer med kreft enn hos dem uten.
Forskerne undersøkte også muligheten for å integrere GEMINI med en tidligere test kjent som DELFI (DNA evaluation of fragments for early interception),
Totalt identifiserte GEMINI og DELFI kreftsvulster korrekt i 91% av tilfellene i 89 prøver.
Bemerkelsesverdig nok oppdaget GEMINI-testen avvik i cfDNA-mutasjonsprofilene flere år før standarddiagnosen hos sju pasienter som ikke hadde noen påvisbare svulster på tidspunktet for blodprøvetakingen.
Seks testet positivt med GEMINI og fikk senere diagnosen lungekreft mellom 231 og 1868 dager etter at prøvene ble tatt.
Fordeling av studien
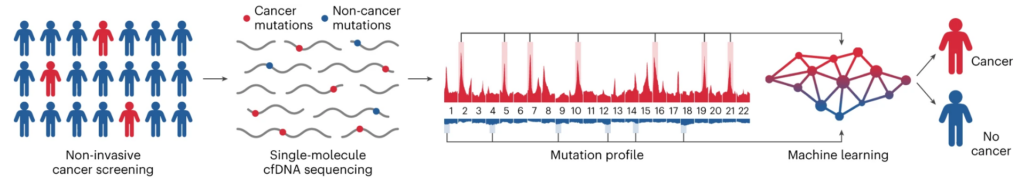
- Blodprøvetaking: En blodprøve tas fra en person som kan være i risikosonen for å utvikle kreft. Denne prøven inneholder cfDNA, små DNA-fragmenter som har blitt skilt ut av celler i kroppen, inkludert potensielle tumorceller.
- DNA-ekstraksjon og sekvensering: cfDNA ekstraheres fra blodprøven og sekvenseres deretter. Det betyr at forskerne kartlegger rekkefølgen på "byggesteinene" som DNA-et består av. Dette hjelper dem med å identifisere eventuelle endringer eller mutasjoner i DNA-et.
- Analyse av DNA-forandringer: Hvert enkelt DNA-molekyl analyseres for eventuelle sekvensendringer, slik at forskerne kan kartlegge mutasjonsprofiler over hele genomet. I bunn og grunn leter de etter mønstre i mutasjonene som kan tyde på kreft.
- Maskinlæring: En maskinlæringsmodell, som er trent opp til å gjenkjenne forskjellen mellom kreftfremkallende og ikke-kreftfremkallende mutasjonsfrekvenser i ulike områder av genomet, brukes deretter til å analysere mutasjonsprofilene. Maskinlæringsmodellen gir deretter en poengsum fra 0 til 1, der en høyere poengsum indikerer en høyere sannsynlighet for kreft.
- Ytterligere validering og testing: Hvis GEMINI-poengsummen er høy, noe som tyder på kreft, brukes tilleggstester som datatomografi og DELFI-testen (som påviser endringer i størrelsen og fordelingen av cfDNA-fragmenter i genomet) for å bekrefte diagnosen og påvise kreftstadiet. Denne kombinasjonen av tester har vist seg å være svært effektiv, og over 90% av lungekrefttilfellene i studien ble oppdaget.
Dette er nok en spennende studie som avslører en ny anvendelse av maskinlæring i medisinsk diagnostikk, denne gangen for å analysere kreft på cellenivå.
Det kreves større kliniske studier for å validere verktøyet før det kan bli tilgjengelig for klinisk bruk.
Denne uken har en AI-støttet brystkreftscreening arbeidsflyten forbedret hastigheten og effektiviteten i vurderingen av mammografier for kreft.